
 |
CHIMICA: LE PROPRIETA' COLLIGATIVEAUTRICE: ILARIA VOLPInumero di matricola 0000281286 |
| |
l'innalzamento ebulloscopico |
|||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
L'INNALZAMENTO EBULLOSCOPICoL'innalzamento
ebulloscopico è la variazione della temperatura di
ebollizione di un solvente dovuta alla presenza di un soluto in
soluzione.
La tensione di vapore (che indica la tendenza all'evaporazione) di una soluzione è minore della tensione di vapore del solvente puro, pertanto è necessario maggior calore per far sì che la pressione del vapore del solvente provochi l'ebollizione della soluzione. Di conseguenza si avrà un innalzamento della temperatura di ebollizione. La variazione della temperatura di ebollizione è proporzionale alla costante ebulloscopica molale (Keb) determinata sperimentalmente, alla molalità (numero moli di soluto su Kg di solvente) e a i (numero di moli che ogni mole di soluto libera in soluzione) secondo questa legge: ΔTeb =
Keb * m * i
 |
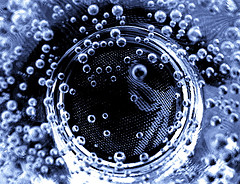 Acqua in ebollizione all'interno di un beaker. |
|||||||||||||||||||||||||||||
COMPOSTI, TEMPERATURE DI EBOLLIZIONE E COSTANTI EBULLOSCOPICHEIn questa tabella sono registrati alcuni composti comuni in laboratorio con le relative temperature d'ebollizione e costanti ebulloscopiche.
 |
||||||||||||||||||||||||||||||
GRAFICO
DELLE TEMPERATURE DI EBOLLIZIONE DI ACQUA
Il
presente grafico mostra
l'aumento delle temperature di ebollizione di soluzioni con
acqua,
etere etilico e benzene |
||||||||||||||||||||||||||||||
|
MOLALITA' |
TEMPERATURA DI |
TEMPERATURA DI EBOLLIZIONE ETERE ETILICO (gradi centigradi) |
TEMPERATURA DI EBOLLIZIONE BENZENE (gradi centigradi) |
|
0 |
100 |
34,55 |
80,1 |
|
10 |
105,15 |
54,75 |
105,4 |
|
20 |
110,3 |
74,95 |
130,7 |
|
30 |
115,45 |
95,15 |
156 |
|
40 |
120,6 |
115,35 |
181,3 |
|
50 |
125,75 |
135,55 |
206,6 |
