COMPOSTI,
TEMPERATURE DI FUSIONE E COSTANTI CRIOSCOPICHE
In
questa tabella sono
registrati alcuni composti comuni in laboratorio con le relative
temperature di fusione e costanti crioscopiche.
|
COMPOSTO
|
PUNTO
DI FUSIONE (gradi centigradi)
|
Kcr
|
|
Acqua
|
0,00
|
1,853
|
|
Acido acetico
|
16,66
|
3,90
|
|
Benzene
|
5,53
|
5,12
|
|
P-xilene
|
13,26
|
4,3
|
|
Naftalene
|
80,29
|
6,94
|
|
Cicloesano
|
6,54
|
20,0
|
|
Tetracloruro di carbonio
|
-22,95
|
29,8
|
|
Canfora
|
179,80
|
40
|

|
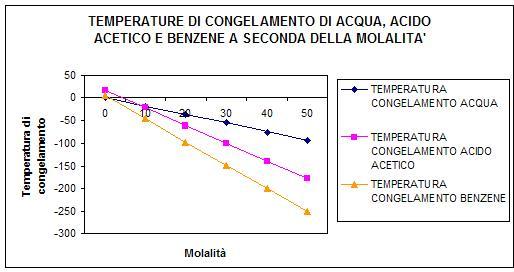
GRAFICO DELLE
TEMPERATURE DI CONGELAMENTO DI ACQUA, ACIDO ACETICO E BENZENE A SECONDA
DELLA MOLALITa'
Il
presente grafico mostra la
diminuzione delle temperature di congelamento di soluzioni con
acqua, acido acetico e benzene con un
soluto (che si è ipotizzato non si dissoci in soluzione) in
funzione
della molalità della soluzione.
| MOLALITA'
(n moli soluto/Kg solvente)
|
TEMPERATURA
CONGELAMENTO
ACQUA (gradi centigradi)
|
TEMPERATURA
CONGELAMENTO
ACIDO ACETICO (gradi centigradi)
|
TEMPERATURA
CONGELAMENTO BENZENE (gradi centigradi)
|
|
0
|
0
|
16,66
|
5,53
|
|
10
|
-18,53
|
-22,34
|
-45,67
|
|
20
|
-37,06
|
-61,34
|
-96,87
|
|
30
|
-55,59
|
-100,34
|
-148,07
|
|
40
|
-74,12
|
-139,34
|
-199,27
|
|
50
|
-92,65
|
-178,34
|
-250,47
|

|

